Introducción
Las baterías de plomo-ácido son uno de los tipos más comunes de baterías utilizadas en diversas aplicaciones. Es necesario comprender el principio básico de las baterías de plomo-ácido para hacer un buen uso de ellas en diversas aplicaciones, como la automoción o las fuentes de energía ininterrumpida. Aumentar la familiaridad con estos conceptos puede mejorar la capacidad de mantenerlos adecuadamente y al mismo tiempo maximizar su potencial para un rendimiento óptimo bajo demanda en diferentes entornos/contextos. Este artículo explora las reacciones químicas en el mecanismo de flujo de iones necesarias para controlar los procesos de carga y descarga.
Reacción química de los electrodos positivos y negativos.
El funcionamiento de las baterías de plomo-ácido implica reacciones químicas en sus dos electrodos primarios: el electrodo positivo, compuesto de dióxido de plomo, y el electrodo negativo, de plomo puro. Comprender el funcionamiento de la batería comienza con su diseño y construcción.
Cuando se expone al ácido sulfúrico junto con otro compuesto llamado "dióxido de plomo" en el electrodo positivo, este procedimiento da como resultado la producción de "iones de oxígeno", así como una amalgama llamada "sulfato de plomo". A la misma velocidad, el plomo puro se combina con el ácido sulfúrico para formar iones de hidrógeno y produce sulfato de plomo. Como resultado de la serie de eventos descritos anteriormente, la energía química se convierte en energía eléctrica, que se utiliza para diversos fines en la sociedad moderna.
El flujo de iones en una solución electrolítica
Es fundamental introducir una solución electrolítica para permitir un intercambio iónico eficaz entre electrodos marcados positiva y negativamente. Esta solución frecuentemente comprende agua mezclada con ácido sulfúrico que actúa como portador de estos iones. Este compuesto crítico puede respaldar el funcionamiento adecuado de la batería a través de sus iones sulfato (SO₄²⁻), que migran activamente durante cada carga y descarga.
Mientras está en el modo de carga, la corriente eléctrica facilita los movimientos de los compuestos de azufre cargados que se disuelven en electrolitos dentro de una batería típica a través de trazas cargadas positivamente, pasando a regiones o trazas cargadas negativamente mediante la acción electrolítica. Esta actividad transformacional revierte la formación de conversión que obstaculizó el almacenamiento anterior al transformar estados sólidos en fluidos a través del ciclo de carga-descarga. Por lo tanto, la restauración gradual permite que estas baterías sean lo suficientemente capaces de almacenar cargas eléctricas de forma segura con diversas capacidades de almacenamiento en diversas aplicaciones.
Esquema y descripción del proceso de carga y descarga.
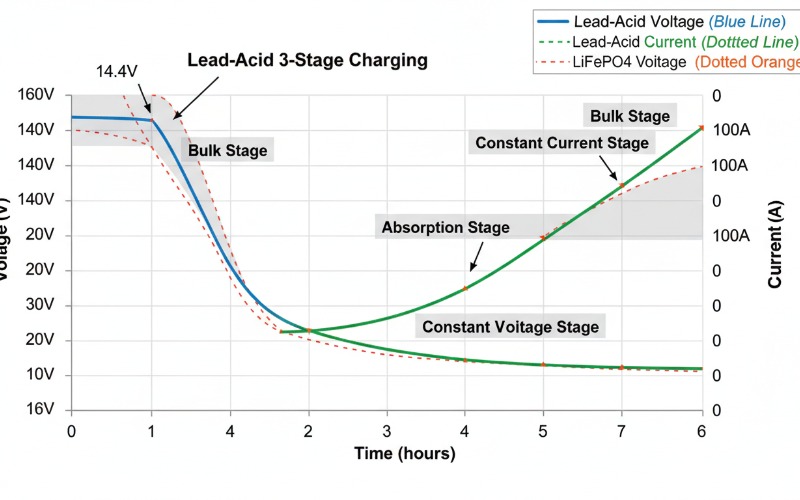
Comprender con precisión cómo se recargan las baterías recargables, como las que utilizan el diseño de plomo-ácido, puede parecer complicado, pero puede ser más manejable cuando se visualiza mediante descripciones esquemáticas. En esencia, observamos que la carga requiere alimentación desde un suministro eléctrico externo para que pueda tener lugar una reacción química interna en la que regiones inactivas como el sulfato de plomo se reorganizan nuevamente en sustancias químicas activas, como plomo puro o dióxido de plomo, lo que permite un almacenamiento de energía renovado en esas celdas de nuestras baterías recargables.
A medida que descarga energía eléctrica en un circuito externo, una batería sufre una transformación química: su ácido sulfúrico reacciona con plomo puro y dióxido de plomo para producir grandes cantidades de sulfato de plomo. Este proceso consume constantemente la energía almacenada del dispositivo hasta que su voltaje disminuye por completo, lo que requiere una recarga inmediata para su uso posterior con regularidad.
La conclusión
En resumen, el conocimiento sobre cómo funcionan las baterías de plomo-ácido es fundamental para maximizar su productividad y longevidad. El factor clave que contribuye a su funcionalidad general es la multitud de reacciones químicas que ocurren en ambos polos junto con el flujo de iones a través de su solución electrolítica durante los ciclos de carga y descarga.









 en
en  ara
ara  de
de  fra
fra  kor
kor  ru
ru  spa
spa  vie
vie